Cl>N。
N和Cl的非金属性应该从电负性比较,电负性大的非金属强。
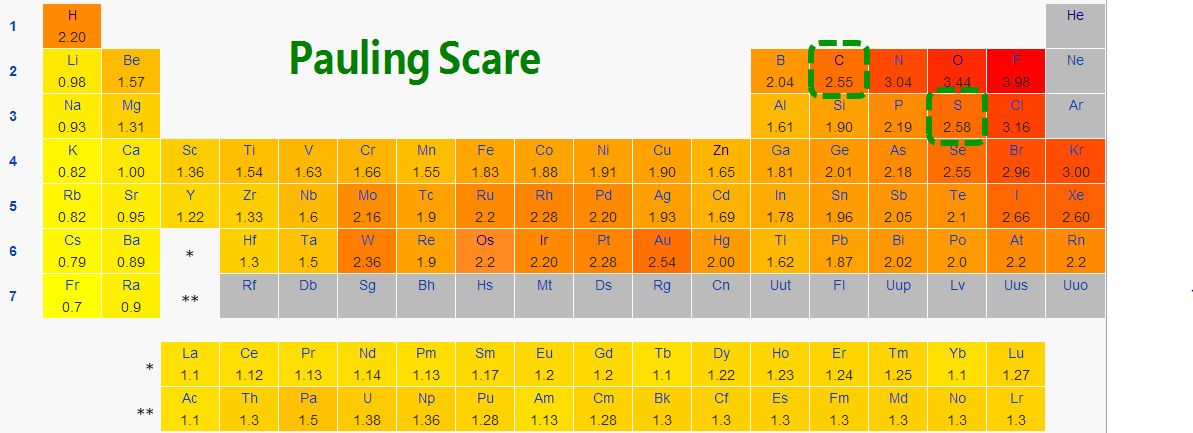
查表:N=3.04,Cl=3.16.(数据比较权威,是鲍林电负性值,这是化学界公认的数值。其中F最大,定为3.98),由此知非金属性:Cl>N。
电负性:指分子中原子吸引电子的能力,或分子中的成键原子对共用电子对的吸引能力。这种能力只能放到分子中去考察,不能孤立的看。
当然可以通过其它方法:如最高价氧化物水化物的酸性,气态氢化物的稳定性等去比较。
扩展资料
电负性的变化规律:
1、随着原子序号的递增,元素的电负性呈现周期性变化。
2、同一周期,从左到右元素电负性递增,同一主族,自上而下元素电负性递减。对副族而言,同族元素的电负性也大体呈现这种变化趋势。因此,电负性大的元素集中在元素周期表的右上角,电负性小的元素集中在左下角。
3、电负性越大的非金属元素越活跃,电负性越小的金属元素越活泼。氟的电负性最大(4.0),是最容易参与反应的非金属;电负性最小的元素(0.79)铯是最活泼的金属。
4、过渡元素的电负性值无明显规律。
参考资料来源:百度百科-电负性